试题详情
- 简答题 25 ℃时,电池Zn|ZnCl2(0.555mol·kg-1)|AgCl(s)|Ag的电动势E=1.015V。已知EΘ(Zn2+|Zn)=-0.7620V,EΘ(Cl-|AgCl|Ag)=0.2222V,电池电动势的温度系数为:
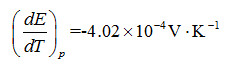 (1)写出电池反应; (2)计算反应的标准平衡常数K; (3)计算电池反应的可逆热Qr,m; (4)求溶液中ZnCl2的平均离子活度因子γ±。
(1)写出电池反应; (2)计算反应的标准平衡常数K; (3)计算电池反应的可逆热Qr,m; (4)求溶液中ZnCl2的平均离子活度因子γ±。
-

关注下方微信公众号,在线模考后查看

热门试题
- 为什么说硝酸钠、硝酸钾在水溶液中一般不参
- 所有自发进行的反应都是放热反应。
- 在一个循环过程中,物系经历了i步变化,则
- 气固相反应CaCO3
- 舞台上经常用喷撒干冰的方法制造白雾以渲染
- 1.00mol(单原子分子)理想气体,
- 啤酒是生活中常见的饮料,其中含有二氧化碳
- 简述可逆途径的特点。
- 杠杆规则只适用于T~x图的两相平衡区。&
- 对于理想气体自由膨胀过程,下述提法正确的
- 用三氯化铝AlCl3
- 某二组分物系气液平衡相图如下图所示,某人
- 在101.325KPa下,水-乙醇二元气
- 在373K下,反应A(g)=B(g)+C
- 加入惰性气体对哪一个反应能增大其平衡转化
- 25℃时将0.568g碘溶于50cm
- 298K和标准压力下,有两瓶萘的苯溶液,
- 80℃时纯苯的蒸气压为100kPa,纯甲
- 稀溶液反应 CH2
- 憎液溶胶有哪些特征?