试题详情
- 简答题某容器中含有14.0gN2、16.0gO2、4.40gCO2时容器的压力为200kPa,计算各气体的分压和该容器得体积。
-
该容器中各气体的物质的量分别为:

各气体的摩尔分数为: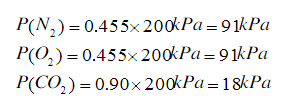

各气体的分压为:
根据气体状态方程pV = nRT得:
关注下方微信公众号,在线模考后查看

热门试题
- 威廉逊(Williamson)合成法是用
- 正常血液中的pH值为7.41,求血液中m
- 关于原子轨道的下列叙述正确的是()
- 量子力学的一个轨道是什么?()
- 化学反应商Q和标准平衡常数的单位均为1。
- 国际理论和应用化学联合会把 的名称定为
- 当CaF2固体溶于
- 向含有CCu2+<
- 胶体粒子为什么会带电?FeOH
- 下列离子能与I 发生氧化还原反应的是:(
- SiHCl3分子根
- 严格地说,理想气体状态方程和分压定律都只
- 根据Mg(OH)2
- 某气体反应,一定温度下达平衡时各物质分压
- 下列各组均为状态函数的是()
- 按IUPAC法,具有CH3
- 某温度时,反应的标准平衡常数则反应的标准
- BF3分子的空间的
- 什么是屏蔽效应和钻穿效应?他们对原子轨道
- 在量子力学中,原子轨道是指电子在核外运动