试题详情
- 简答题 将下列反应组成原电池(温度为298.15K): 2I-(aq)+2Fe3+(aq)===I2(s)+2Fe2+(aq) (l)计算原电池的标准电动势; (2)计算反应的标准摩尔吉布斯函数变; (3)用图式表示原电池; (4)计算c(I-)=1.0×10-2mol˙L-1以及c(Fe2+/10时原电池的电动势。
-
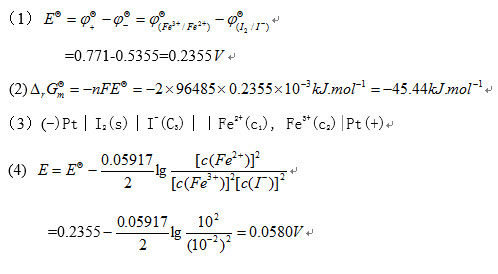
关注下方微信公众号,在线模考后查看

热门试题
- 已知氨水溶液的浓度为0.20mol˙L
- 反应活化能越大,反应速率也越大。
- 计算说明c(NaAc)=0.10 mol
- 下列物质中能使石蕊由蓝变红的是:()
- 计算含有0.100mol.dm
- 稀溶液的依数性
- 易于形成配离子的金属元素是位于周期表中的
- 氧化性强弱正确的顺序是()。
- 3个p轨道的能量、形状和大小都相同,不同
- 某基元反应2A(g)+B(g)=C(g)
- 在CaF2的饱和溶
- HgCl2分子中H
- 抑制FeCl3水解
- 如果一反应的活化能为117.5 kJ·m
- 多原子分子中,键的极性和分子极性()。
- 利用下列两个反应及其值,计算Fe
- 用杂化轨道理论预测下列分子的空间构型,其
- 天然橡胶是什么的聚合物?()
- 写出Cu的核外层电子排布式。
- 101℃下,水沸腾时的压力是:()