试题详情
- 简答题用银电极电解KCl水溶液。电解前每100g溶液中含KCl 0.7422g。阳极溶解下来的银与溶液中的Cl-反应生成AgCl(s),其反应可表示为
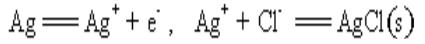 总反应为
总反应为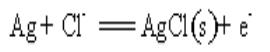 通电一定时间后,测得银电量计中沉积了0.6136g Ag,并测知阳极区溶液重117.51g,其中含KCl 0.6659g。试计算KCl溶液中的t(K+)和t(Cl-)
通电一定时间后,测得银电量计中沉积了0.6136g Ag,并测知阳极区溶液重117.51g,其中含KCl 0.6659g。试计算KCl溶液中的t(K+)和t(Cl-)

关注下方微信公众号,在线模考后查看

热门试题
- 催化剂在反应前后所有性质都不改变。
- “反应平衡常数改变了,化学平衡一定会移动
- 乳状液必须有乳化剂存在才能稳定。
- 若用γ和a2分别表
- 燃料煤所产生的(二氧化硫)是产生酸雨的主
- 恒温恒压下,物质A与物质B形成均相溶液系
- 已知1mol HCl的无限稀
- 一定温度、压力下,化学反应Ag(s)+1
- 临界温度高的气体()
- 如果要你测定某强电解质的极限(无限稀)摩
- 破坏臭氧的反应机理为:NO+O→NO
- 公式W膨=C
- 泡沫是以()为分散相的分散系统。
- 理想液态混合物分子间无相互作用力,分子不
- 已知25℃时,NH4
- 下列反应AgCl(s)+I-<
- 对大多数系统来讲,当温度升高时,表面张力
- 循环过程不一定是可逆过程( )
- 相图与相律之间是什么关系?()
- 试分别由生成焓和燃烧焓计算下列反应: