试题详情
- 简答题有如下几个化学反应计量式,分别写出用参与反应的各种物质表示的速率表示式。设反应都是基元反应,根据质量作用定律写出反应的速率方程。 (1)A+B=C (2)2A+B=2C (3)A+2B=C+2D (4)2CL+M=CL2+M
- 化学反应速率的定义式为
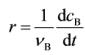 ,用参与反应的任意一种物质表示的速率,都应该有相同的结果。基元反应的速率与各反应物浓度的幂乘积成正比,其中各浓度项的方次即为反应方程中各种物质的计量系数,这就是质量作用定律,质量作用定律只适用于基元反应。所以
,用参与反应的任意一种物质表示的速率,都应该有相同的结果。基元反应的速率与各反应物浓度的幂乘积成正比,其中各浓度项的方次即为反应方程中各种物质的计量系数,这就是质量作用定律,质量作用定律只适用于基元反应。所以
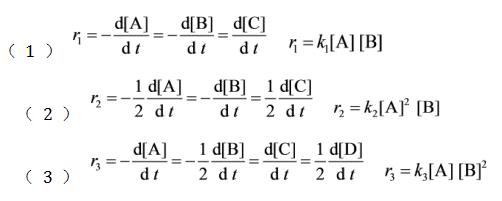
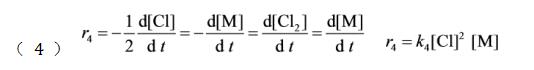
关注下方微信公众号,在线模考后查看

热门试题
- 某等容反应的正向反应活化能为E
- 大分子溶液与溶胶一样是多相不稳定体系。
- 什么是自发过程?什么是热力学第二定律?
- 在101.325kPa的大气压力下,将蔗
- 宏观测定的某种物理量实际上是相应微观量的
- 实验测得NO在Pt上的催化分解反应:2N
- 1.00mol氧在30℃下从0.10MP
- B物质在α相中浓度大于在β相中的浓度,当
- 设范德华气体方程中,常数a和b均大于零。
- 某反应的速度常数k=4.62×10
- 已知 445℃时,Ag
- 单分子层吸附只能是化学吸附,多分子层吸附
- 理想气体从同一始态(p1、V1、T1)出
- 分解电压就是能够使电解质在两极上持续不断
- 用同一滴管分别滴下1cm3
- 为了保证施工质量,冬季建筑施工中常在浇注
- 一直到1000pө
- 1mol单原子理想气体从300K、300
- 在相图上,当体系处于下列哪一点时只存在一
- 可同时称为偏摩尔量与化学势的偏微商是()