试题详情
- 简答题对比等电子体CO与N2的分子结构及主要物理、化学性质。
-
CO和N2是等电子体(14e),分子轨道能级图相似,分子中都有三重键:∶N≡N∶、
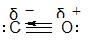 ,键能相近。一般条件下,两种物质都是气体,很少溶于水;熔、沸点,临界压力,临界温度等一些物理性质也相似。
,键能相近。一般条件下,两种物质都是气体,很少溶于水;熔、沸点,临界压力,临界温度等一些物理性质也相似。
但CO和N2分子中三重键特点并不完全相同,N2分子中负电荷分布是对称的,而CO却是不对称的。C原子略带负电荷,再加上C的电负性比N小,因此CO比N2较易给出电子对向过渡金属原子(离子)配位,除形成σ―配键外,还有π―反馈键形成,故生成的配合物较稳定。而N2的配位能力远不如CO,分子氮配合物远不如羰基化合物稳定。所以CO的键能虽比N2略大,但化学性质却比N2要活泼,不像N2那样“惰性”。 关注下方微信公众号,在线模考后查看

热门试题
- 碱金属在什么条件下存在双原子分子?为什么
- 0.10 moldm-3
- 在1100K,下面那种物质能把Cr
- 稀有气体氙能与下列哪种元素形成化合物()
- 下列多电子原子能级在电子填充时能量最高的
- 50ml0.2mol/LAlCl
- 请解释下列有关键长和键角的问题:在N
- 制备HF的主要方法是()作用,其反应方程
- 造成部分地区酸雨的主要大气污染物是()。
- 下列掺杂半导体属于n型半导体的是()
- 锡`铅的氢氧化物表现出两性,按下图所示方
- 根据酸碱质子理论,下列物质既可作酸又可作
- 碳族元素中,碳和其它元素相比性质差异较大
- 有人推测尚未合成的第114号元素有相当稳
- 关于ⅠB族性质叙述不正确的是()
- MO法中成键电子数与反键电子数之差的一半
- 在纯水和浓度都是0.1mol&bull
- Rh(CO)4H的
- 简单离子的电子层构型(除2e.8e,18
- 在1.0L0.1mol·L-1