试题详情
- 简答题 化学反应HC2O4–(ag)+C6H5O–(ag) === C2O42–(ag)+C6H5OH(ag) (1)计算反应在298.15 K时的ΔrGmΘ(298.15); (2)当反应物的浓度皆为0.01mol·L–1,生成物的浓度皆为0.1mol·L–1时,反应向哪个方向进行? (已知H2C2O4 Ka2Θ=6.4×10–5,C6H5OH的KaΘ=1.0×10–10)
-

(2)反应商: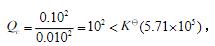 所以反应正向进行。
所以反应正向进行。
(或根据rGm的正、负判断:rGm==ΔrGmΘ+RTLnQ= –32.84+RTln100 = –32.84+11.41= –21.43(kJ·mol–1
)<0。 关注下方微信公众号,在线模考后查看

热门试题
- 一元弱酸弱碱盐水溶液的酸度与溶液的浓度无
- 在1100K,下面那种物质能把Cr
- 对于所有零级反应来说,下列叙述正确的是(
- 难溶电解质的Kθ<
- 有五瓶白色粉末,没有标签,但知道它们是M
- 下列分子中偶极矩为零的是()
- A→B+C 是吸热的可逆基元
- 某化学反应速度常数的单位是mol·L
- 已知:Ag2S的溶
- 请回答下列有关氮元素性质的问题:为什么氮
- 在Fe3+离子的溶
- 为何氮气是反磁性物质而氧气却是顺磁性物质
- 电池反应为:PbSO4
- 为防止1 dm3<
- 为什么当硝酸与[Ag(NH3<
- 回答下列有关硝酸的问题:根据HNO
- 在[Pt(NH3)
- 二氧化铅具有两性,酸性大于碱性.它与碱作
- 在732K时反应NHCl(s)NH
- ⅡB族金属与稀盐酸和稀硫酸反应缓慢的是(