试题详情
- 简答题有两个反应,其活化能分别为E1=41.84kJ•mol-1,E2=167.4kJ•mol-1,在0℃时若使反应速率常数加倍,计算每个反应需升高的温度。
-
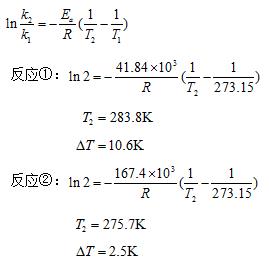
关注下方微信公众号,在线模考后查看

热门试题
- 如图所示,a、b、c为内径相同的玻璃毛细
- 室温下一高压釜内有常压的空气,为进行实验
- 当系统向环境传热时(Q <&
- 某系统经历一不可逆循环过程,下列答案中错
- 某一基元反应的动力学方程为r=kc
- 苯和甲苯在298.15K时蒸气压分别为
- 在电解质溶液中,如果有i种离子存在,则溶
- CO2与H
- 典型的憎液溶胶才能全面地表现出胶体的三个
- 摩尔理想气体的是()
- 欲研究某化学反应的反应截面和它与反应速率
- 对于理想气体,下列哪个关系是不成立的()
- 化学反应CO2(g
- 用一个每毫米有1000条缝的平面衍射光栅
- 什么是最低恒沸混合物?什么是最低恒沸点?
- 若已知H2O(g)
- 无限稀电解质溶液的摩尔电导率可以看成是正
- 请给出两个你认为最重要的麦克斯韦关系式,
- 100℃、101325 Pa
- 对于平行反应已知活化能E1>E2,请问