试题详情
- 简答题一容器中有4.4g CO2,14g N2和12.8g O2,气体总压为2.026×105Pa,求各组分的分压。
-
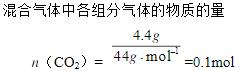

关注下方微信公众号,在线模考后查看

热门试题
- 用氦核轰击Al-27核时,得到P-30和
- 在H2O
- 第118号元素原子的最外层电子构型应为(
- 现有一白色固体A,溶于水产生白色沉
- 下列金属的碳酸盐不易溶于水的是()
- 钻石所以那么坚硬是因为碳原子间都是共价键
- 计算表明,CO、NO的分子轨道能级图中的
- Cu2+能氧化()
- 根据分子轨道理论,O2
- 试用价层电子互斥理论判断下列分子或离子的
- 氢原子核外电子光谱中的莱曼光谱中有一条谱
- 从标准电极电势看K比Na活泼,但为什么N
- 工业上制备CO的主要方法是().造成人体
- 下列氧化物中单独加热到温度不太高时能放出
- 一敞开烧瓶在280K时充满气体,要使1/
- M2+离子的3d轨
- 下列分子中,同时存在σ键和π键的是()。
- 下列化合物哪个熔沸点最低()
- 将NO2气体降温,
- 下列Lewis酸中,酸性最强的是()