试题详情
- 简答题通C12于消石灰中,可得漂白粉,而在漂白粉溶液中加入盐酸可产生C12,试用电极电势说明这两个现象。
-

当C12通入消石灰溶液中时是碱性介质, C12可发生歧化反应:
C12可发生歧化反应:
2C12+2Ca(OH)2=Ca(C1O)2+CaC12+2H2O
得到的产物是漂白粉。加盐酸到漂白粉溶液中,使体系酸化,此时,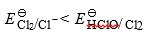 ,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:
,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:
Ca(C1O)2+4HCl=2Cl2+CaC12+2H2O
所以,上述两个反应是介质酸碱性的变化导致某些氧化还原反应方向改变的例证。 关注下方微信公众号,在线模考后查看

热门试题
- SO2的漂白作用与
- 下列两性氢氧化物中,碱性最强的是()
- 将NO2气体降温,
- 当温度升高至某一温度时,离子表面活性剂在
- 下列各组溶液中,在相同温度下渗透压相等的
- 一个半反应式NO3
- 0℃ 和标准压力下,1dm<
- 某反应体系的温度一定时,当反应物的一部分
- 已知298K时,Kθ
- 写出24号元素的电子排布式,并指出该元素
- 硼的独特性质表现在()。
- 将1.01g胰岛素溶于适量水中配制成10
- 欲使100毫升纯水的pH值由7变为4,所
- 除氟外,各种卤素都可以生成几种含氧酸根,
- 反应N2(g)+O
- 用价层电子对互斥理论估计COCl
- 对于4p1电子,下
- 根据价层电子对互斥理论,XeF
- 下列各电子对中,电对的代数值最小的是()
- 写出下列反应方程式,并注明产物颜色:向K