试题详情
- 简答题称取1.250g纯一元弱酸HA,溶于适量水后稀至50.00mL,然后用0.1000mol/LNaOH溶液进行电位滴定,从滴定曲线查出滴定至化学计量点时,NaOH溶液用量为37.10mL。当滴入7.42mLNaOH溶液时,测得pH=4.30。计算:一元弱酸HA的摩尔质量
-
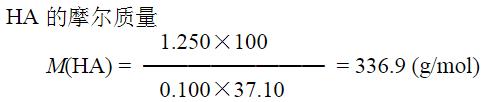
关注下方微信公众号,在线模考后查看

热门试题
- 已知将反应 Ag+
- 在苯和H2O分子间存在着()
- 某一元弱酸(HA)试样1.250g,加水
- 对某一样品进行分析:A测定结果的平均值为
- pH=10.20含有()位有效数字,Fe
- 下列化合物中不水解的是()
- 人体血液中最主要的缓冲对为()。正常人血
- 在火焰原子化过程中,伴随着产生一系列的化
- 什么叫状态函数?什么叫广度性质?什么叫强
- (1)用0.02mol/L KMnO<
- 已知:计算O-H键的键能EO-
- 在阳离子第四组与第五组鉴定中,主要是加入
- 欲配制草酸钠溶液用以标定0.04mol/
- 在pH为10.0的氨性溶液中,已计算出α
- 化学纯试剂可用于()。
- 在pH=10的氨性缓冲溶液中,用EDTA
- 为防止配制的SnCl2
- 易挥发溶质溶于溶剂之后可能会引起()
- 玻璃器皿的洗涤可根据污染物的性质分别选用
- 试判断: 反应C6