试题详情
- 简答题在25℃,101.3kPa下,CaSO4(s)=CaO(s)+SO3(g),已知该反应的
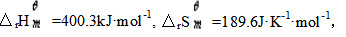 问: (1)在25℃时,通过计算说明上述反应在能否自发进行? (2)对上述反应,是升温有利,还是降温有利? (3)计算上述反应的转折温度。
问: (1)在25℃时,通过计算说明上述反应在能否自发进行? (2)对上述反应,是升温有利,还是降温有利? (3)计算上述反应的转折温度。

关注下方微信公众号,在线模考后查看

热门试题
- 分子轨道理论对物质的顺磁性是如何解释的?
- 双原子分子的键能就是它的()。
- 原电池中正极进行()反应,电解池中()极
- 两种分子酸HX溶液和HY溶液有相同的pH
- 由标准钴电极(Co2+
- 在原电池中,下列叙述正确的是哪个?()
- 试计算下列情况的热力学能变化: (1)
- 乙醇和二甲醚(CH3
- 试计算25℃时0.10mol·dm
- 下列两反应中,Mg+2Ag+<
- 已知298K时, 2NH3<
- 催化剂能改变反应历程,降低反应的活化能,
- 应用于弗瑞迪尔-克拉夫茨(Friedel
- 由偶极诱导产生的分子间作用力称为:()
- 速度方程式中,各种物质浓度的指数等于反应
- 下列化合物中属于共价型化合物的是:()
- 在200克水中溶解100克乙二醇C
- 关于液晶,下列说法正确的是哪个?()
- 某基元反应2A(A)+B(g)===C(
- 下列分子间只存在色散力、诱导力和取向力的