试题详情
- 简答题 25℃时,电池Pt│H2(g,100kPa)│H2SO4(b)│Ag2SO4(s)│Ag的标准电动势EΘ=0.627V。已知EΘ(Ag+│Ag)=0.7994V。 (1)写出电极反应和电池反应; (2)25℃时实验测得H2SO4浓度为b时,上述电池的电动势为0.623V。已知此H2SO4溶液的离子平均活度因子γ±=0.7,求b为多少; (3)计算Ag2SO4(s)的活度积。
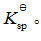
-

关注下方微信公众号,在线模考后查看

热门试题
- 某一基元反应的动力学方程为r=kc
- 如图所示一带隔板的容器中,两侧分别有同温
- 不能用于测定溶液pH值的电极是:()
- 书写化学方程式应遵守哪些原则?
- 可逆电池反应的ΔH与反应热Q不相等。
- 沸点和恒沸点有何不同?
- 弯曲表面上附加压力的计算公式:̳
- 有电池Cu(s)│Cu(Ac)
- 实际电解时,在阴极上首先发生还原作用而放
- 催化剂为什么能加快反应速率?
- 原电池Pt,H2(
- 在413K时,纯C6
- 直径为1μm的石英微尘,从高度为
- 理想气体从相同的始态出发分别进行恒温可逆
- O2(g)的的标准
- 反应A+B→C+D的速率方程为r=k[A
- 能证明科尔劳乌施经验式(Λm<
- 金属与盐符合什么具体条件才能发生置换反应
- 氢气进行不可逆循环()
- 已知H+&ensp