试题详情
- 简答题利用电极电势解释下列现象:在淀粉碘化钾溶液中加入少量NaClO时,得到蓝色溶液A,加入过量NaClO时,得到无色溶液B,然后酸化之并加少量固体Na2SO3于B溶液,则A的蓝色复现,当Na2SO3过量时蓝色又褪去成为无色溶液C,再加入NaIO3溶液蓝色的A溶液又出现。指出A、B、C各为何种物质,并写出各步的反应方程式。
-
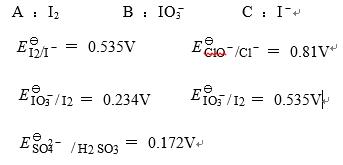
加少量NaClO后,由于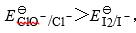 所以I-被ClO-氧化为I2(蓝色),当NaClO过量时,由于
所以I-被ClO-氧化为I2(蓝色),当NaClO过量时,由于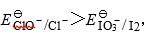 所以I2继续被氧化为IO3-(无色),酸化并加入Na2SO3后,由于
所以I2继续被氧化为IO3-(无色),酸化并加入Na2SO3后,由于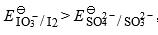 ,所以IO3-被SO32-还原为I2,又显蓝色。当Na2SO3过量时,由于
,所以IO3-被SO32-还原为I2,又显蓝色。当Na2SO3过量时,由于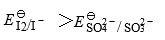 ,所以SO32-能将生成的I2还原为I-。再加入NaIO3后,由于
,所以SO32-能将生成的I2还原为I-。再加入NaIO3后,由于 ,所以IO3-能将I-氧化成I2,本身也被还原成I2,各步反应方程式如下:
,所以IO3-能将I-氧化成I2,本身也被还原成I2,各步反应方程式如下:
(1)ClO-+2I-+H2O=I2+Cl-+2OH-(蓝色A)
(2)5C1O-+I2+2OH-=5Cl-+2IO3-+H2O(无色B)
(3)2IO3-+5SO32-+H2O=I2+5SO42-+H2O(蓝色又复现)
(4)I2+SO32-+H2O=2I-+SO42-+2H+(无色C)
(5)5I-+IO3-+6H+=3I2+3H2O(蓝色A复现) 关注下方微信公众号,在线模考后查看

热门试题