试题详情
- 简答题 25 ℃时水的电导率为5.5×10-6S·m-1,密度为997.0kg·m-2。H2O中存在下列平衡:H2O
 H++OH-,计算此时H2O的摩尔电导率、解离度和H+的浓度。
H++OH-,计算此时H2O的摩尔电导率、解离度和H+的浓度。
-
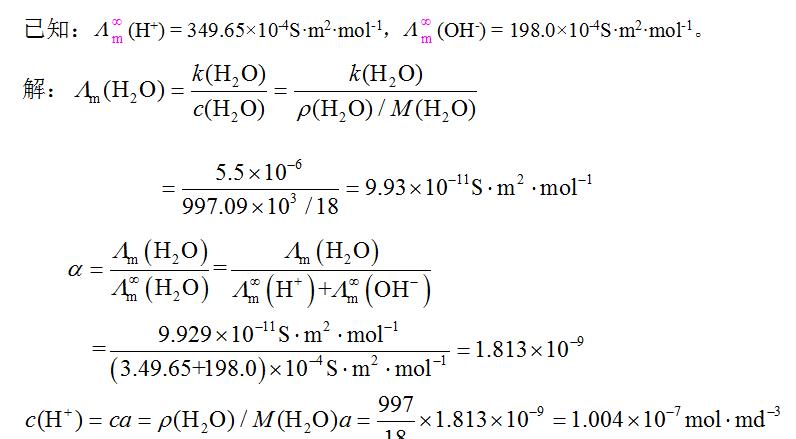
关注下方微信公众号,在线模考后查看

热门试题
- 已知温度为T时,液体A的蒸气压为1333
- 在标准压力pº下,383.15
- 对于反应过程中温度、压力有变化的化学反应
- 为了计算绝热不可逆过程的熵变,可以在始末
- 下列公式皆可用于封闭系统的单纯PVT变化
- 可逆过程的熵永不减少。
- 电池Pb∣H2(1
- 若电池的电池反应电势E〉0,则表明该电池
- Krafft点是何含义?可否利用之?
- 25℃时,用铂电极电解1mol̶
- 稀释强电解质溶液时,其摩尔电导率Λ
- 理想气体的微观模型要点包括()。
- 可燃物燃烧必须符合哪些条件?由此得出灭火
- KI与AgNO3形
- 0.1mol.kg-1
- 已知E1(Fe
- 理想稀溶液中溶剂分子与溶质分子之间只有非
- 光合作用反应6CO2
- 盐桥中使用的电解质需满足的条件是()。
- 如果打开TIME/DIV旋钮下的微调开关