试题详情
- 简答题
背景材料:
阅读下列三段高中化学教学中有关“富集在海水中的元素--氯”的材料。
材料一《普通高中课程标准(实验)》的内容标准:通过实验了解氯、氮、硫、硅等非金属及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响。
材料二以下是某教师设计的教学过程:
[故事导入]
1997年1月8日夜,在巴基斯坦东北部的拉合尔市郊,乌拉姆·吉拉尼驾驶着他那辆旧卡车行驶在莫古尔拉普区那坑洼不平的路上。车上拉的是纺织厂漂白牛仔布用的30多罐氯气,但乌拉姆并不知道氯是什么东西。由于在运货途中他去看了一位朋友,为了节省时间,最后只能抄近道将氯气运到目的地。途中,这辆车的后轮突然卡进了路边的地沟里,乌拉姆急忙前后猛打方向盘,车上的钢瓶被震得叮当乱响。有几只安全系数不合格的钢瓶,在相互碰撞中氯气便发生了泄漏。乌拉姆被氯气的怪味吓坏了,趁着夜深人静溜之大吉。在不到半小时的时间内,黄绿色的杀人烟雾便扩散到方圆几公里并袭击了数百个家庭。原来宁静的夜晚转眼间炸开了锅,人们醒来后睁不开眼又喘不过气,挣扎着冲出屋去,但在一两分钟内又瘫倒在街上……
毒祸共造成20多人死亡,1000多人中毒,巴基斯坦看守政府总理哈立德在9日早晨专程从首都伊斯兰堡飞往拉合尔看望受害者,宣布政府给每个死难家属5万卢比的抚恤,同时制定有关危险品运输方面的法规……
讨论回答:
讨论回答:
1.这是什么气体?
2.这种气体有什么特性?
3.你还在哪儿见识过它?
【实验】引导学生观察集气瓶中氯气的颜色。
【投影】黄绿色气体、有刺激性气味、有毒、易液化。在压强为101kPa、温度为-34.6℃时,氯气液化成液氯。将温度继续冷却到-101℃时,液氯变成固态氯。
【板书】1.与金属反应
【演示实验】铜在氯气里燃烧,并写出反应的化学方程式。
【板书】
 【讲解】CuCl2溶于水,同学们可观察到不同的颜色,这与溶液浓度有关。当CuCl2溶液浓度较大时,溶液呈绿色,当CuCl2溶液浓度较小时,溶液呈蓝色。
【练习】
【板书】2.与氢气反应
【演示实验】H2在Cl2中燃烧(点燃氢气前已先行经过验纯,所以直接点燃氢气,为后面的问题留下伏笔)。
【板书】
【讲解】CuCl2溶于水,同学们可观察到不同的颜色,这与溶液浓度有关。当CuCl2溶液浓度较大时,溶液呈绿色,当CuCl2溶液浓度较小时,溶液呈蓝色。
【练习】
【板书】2.与氢气反应
【演示实验】H2在Cl2中燃烧(点燃氢气前已先行经过验纯,所以直接点燃氢气,为后面的问题留下伏笔)。
【板书】 【讲解】纯净的H2在Cl2中燃烧发出苍白色火焰,生成HCl气体,HCl具有刺激性气味,极易溶于水。HCl的水溶液叫作氢氯酸,亦称盐酸。同学们观察到的白雾就是HCl气体跟空气中的水蒸气结合所形成的盐酸小液滴(酸雾)。盐酸是重要的化工原料。
【板书】3.与水反应:
【讲解】纯净的H2在Cl2中燃烧发出苍白色火焰,生成HCl气体,HCl具有刺激性气味,极易溶于水。HCl的水溶液叫作氢氯酸,亦称盐酸。同学们观察到的白雾就是HCl气体跟空气中的水蒸气结合所形成的盐酸小液滴(酸雾)。盐酸是重要的化工原料。
【板书】3.与水反应: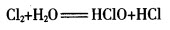 【讲解】氯气溶解于水,在常温下,1体积水约溶解2体积的氯气。溶解的氯气部分能够与水起反应,氯气的水溶液叫“氯水”,氨水因水溶有氯气而呈黄绿色。观察盛在试管中的氯水。
【演示】将一朵红色鲜花放入装有氯气的集气瓶中。
鲜花很快褪色。是Cl2还是HClO使鲜花褪色?
课后思考:溶解于水的氯气只有一部分反应,那么氯水有哪些粒子?如何用实验的方法
一一验证这些粒子的存在?
【板书】4.与碱反应
【讲解】氯气溶解于水,在常温下,1体积水约溶解2体积的氯气。溶解的氯气部分能够与水起反应,氯气的水溶液叫“氯水”,氨水因水溶有氯气而呈黄绿色。观察盛在试管中的氯水。
【演示】将一朵红色鲜花放入装有氯气的集气瓶中。
鲜花很快褪色。是Cl2还是HClO使鲜花褪色?
课后思考:溶解于水的氯气只有一部分反应,那么氯水有哪些粒子?如何用实验的方法
一一验证这些粒子的存在?
【板书】4.与碱反应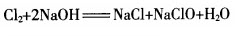 上面的反应可以对照
上面的反应可以对照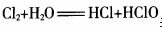 来理解。
工业上用石灰乳制取漂白粉
来理解。
工业上用石灰乳制取漂白粉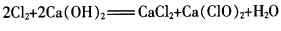
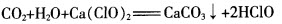 【讨论】根据所学习的氯气的性质,请你提出应对氯气泄漏时的一些简单办法。
【投影】发生氯气泄漏事件时,污染区居民切忌惊慌,应向上风向地区转移,并用湿毛巾护住口鼻;到了安全地带要好好休息,避免剧烈运动,以免加重心肺负担,恶化病情;患者应及时送到大医院或有职业病科的医疗单位,使病人得到有效治疗可以完全康复。
氯气的用途:消毒、制造盐酸、漂白剂、氯仿等有机溶剂、多种农药。
请根据上述材料,完成以下相关任务:
问题: (1)试确定本课的三维教学目标。 (2)分析学情。 (3)试确定本课的教学重难点。 (4)某温度下,将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比是1:2,则Cl:与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是()。 A.2:3 B.4:3 C.10:3 D.11:3
【讨论】根据所学习的氯气的性质,请你提出应对氯气泄漏时的一些简单办法。
【投影】发生氯气泄漏事件时,污染区居民切忌惊慌,应向上风向地区转移,并用湿毛巾护住口鼻;到了安全地带要好好休息,避免剧烈运动,以免加重心肺负担,恶化病情;患者应及时送到大医院或有职业病科的医疗单位,使病人得到有效治疗可以完全康复。
氯气的用途:消毒、制造盐酸、漂白剂、氯仿等有机溶剂、多种农药。
请根据上述材料,完成以下相关任务:
问题: (1)试确定本课的三维教学目标。 (2)分析学情。 (3)试确定本课的教学重难点。 (4)某温度下,将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO-与ClO3-的物质的量浓度之比是1:2,则Cl:与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是()。 A.2:3 B.4:3 C.10:3 D.11:3
-
(1)知识与技能:了解氯气的物理性质;掌握氯气的化学性质;提高实验操作能力,观察能力,分析、推理、归纳能力。
过程与方法:通过探究实验,培养分析问题的能力,设计并完成实验的能力。
情感态度与价值观:感受舍勒的成就和遗憾,体会质疑是科学研究的重点品质:培养透过现象挖掘本质的探究精神。
(2)学生在初中虽然学习了一些元素化合物知识,但是比较肤浅、零散,更没有理论体系。本专题是学生在进入高中学习阶段第一次系统地探究典型元素及其化合物的性质和用途,体现了学科知识与社会实际的有机融合。学生在习得相关的化学知识、实验技能和探究方法的同时,认识到自然资源利用与化学科学密不可分,体会人与自然和谐共处的重要意义。
(3)教学重点:氯气的化学性质。教学难点:氯气的化学性质;培养学生知识应用能力。
(4)D。解析:由已知条件及质量守恒定律写出方程式: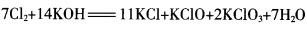 被氧化的氯为3mol,被还原的氯为11mol。即被还原的氯元素与被氧化的氯元素的物质的量之比为11:3。
被氧化的氯为3mol,被还原的氯为11mol。即被还原的氯元素与被氧化的氯元素的物质的量之比为11:3。
关注下方微信公众号,在线模考后查看

热门试题
- 背景材料: 联系学生生活实际创
- 背景材料: 阅读下列三段材料,根据要
- 背景材料: 在体积为VL的密闭
- 背景材料: 阅读下列三段高中化
- 背景材料: 问题: (1)试确定本课
- 背景材料: 在做喷泉实验
- 背景材料: 高中课程要成为每个
- 背景材料: 概念图是由美国康奈
- 背景材料: 在某100mL的混
- 背景材料: 问题: (1)&ldqu
- 背景材料: 某教师在一次
- 背景材料: 以下是《全日制普通高级中
- 背景材料: 随着21世纪的来临
- (1)化学课程目标确立的依据有哪些?(2
- 背景材料: 在做银镜反应的实验时,通
- 背景材料: 某化学教师在讲解&
- 背景材料: 以下是《无机非金属
- 背景材料: 某化学老师在
- 背景材料: 好的新课导入,快速
- 背景材料: 某化学老师在