试题详情
- 简答题
背景材料:
在反应中
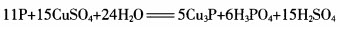 ,每摩尔CuSO4能氧化P的物质的量为()。
A.1/5mol
B.2/5mol
C.3/5mol
D.11/5mol
上面是某教师设计的化学测试中的一道题。
问题: (1)分析学生可能出现的解题错误及原因。 (2)本题正确答案为(),分析其正确的解题思路。
,每摩尔CuSO4能氧化P的物质的量为()。
A.1/5mol
B.2/5mol
C.3/5mol
D.11/5mol
上面是某教师设计的化学测试中的一道题。
问题: (1)分析学生可能出现的解题错误及原因。 (2)本题正确答案为(),分析其正确的解题思路。
-
(1)学生可能错选B。从化学方程式可以看出,15molCuSO4生成6molH3PO4,所以1molCuSO4生成2/5molH3PO4。错解原因:没有注意到生成物中的H3PO4有一半是P自身氧化还原反应(歧化反应)生成的。
(2)本题的正确答案是A。解题思路:题中的还原剂是P,而氧化剂是P和CuSO4。由于反应过程中Cu从+2降为+1,因此反应中共得到15mol的电子:而做还原剂的P在反应中从0升至+5价,因此1molP得到5mol电子。因此15molCuSO4在反应中氧化3mol的P,即每摩尔硫酸铜能够氧化0.2mol的P。 关注下方微信公众号,在线模考后查看

热门试题
- 背景材料: 已知某混合金属粉末
- 小宇是一名高一的学生,他对文科感兴趣,非
- 背景材料: 把aL硫酸铵和硝酸
- 背景材料: 阅读下列三段高中化学教学
- 背景材料: 某化学教师在讲解&
- 背景材料: 以下是李老师的《化学能与
- 背景材料: 阅读下列三段材料,根据要
- ()是教师通过操作实物来帮助学生认识事物
- 背景材料; 化学反应的速率和限
- 背景材料: 某化学老师在一次化学测验
- 背景材料: 阅读下面文字,回答
- 背景材料: 高中课程要成为每个
- 背景材料: 铁是人体必需的微量元素,
- 请对《全日制普通高级中学教科书(必修)
- 背景材料: 《普通高中化学课程
- 背景材料: 高中化学新课程着眼于学生
- 背景材料: 下面是铝热反应的改
- 背景材料: 阅渎下列三段高中化
- 普通高中化学课程标准中提出“积极倡导学生
- 正确地进行化学课堂教学设计实施评价,能够